即将于2026年5月15日实施的《药品管理法实施条例》,标志着我国医药监管体系的一次深层次变革。此次修订不再局限于审批流程或单一主体监管,而是将监管重心延伸至从药品研发、生产到流通、使用的全过程,构建起覆盖全生命周期的监管体系。
这一变化的本质,在于将药品从“审批合格的产品”,转变为“持续受控的风险对象”。监管不再只关注最终结果,而是更加重视过程的可控性与数据的可追溯性。这意味着,企业过去依赖经验和流程管理的方式,将难以满足新的合规要求,取而代之的,是以数据为基础的全流程透明化管理能力。
责任体系重塑:MAH制度推动风险全面上移
在新的监管框架下,药品上市许可持有人(MAH)被确立为全链条的核心责任主体。无论药品的生产、运输还是销售环节是否外包,最终责任均由MAH承担。这一制度设计,从根本上改变了过去多主体分散责任的格局。
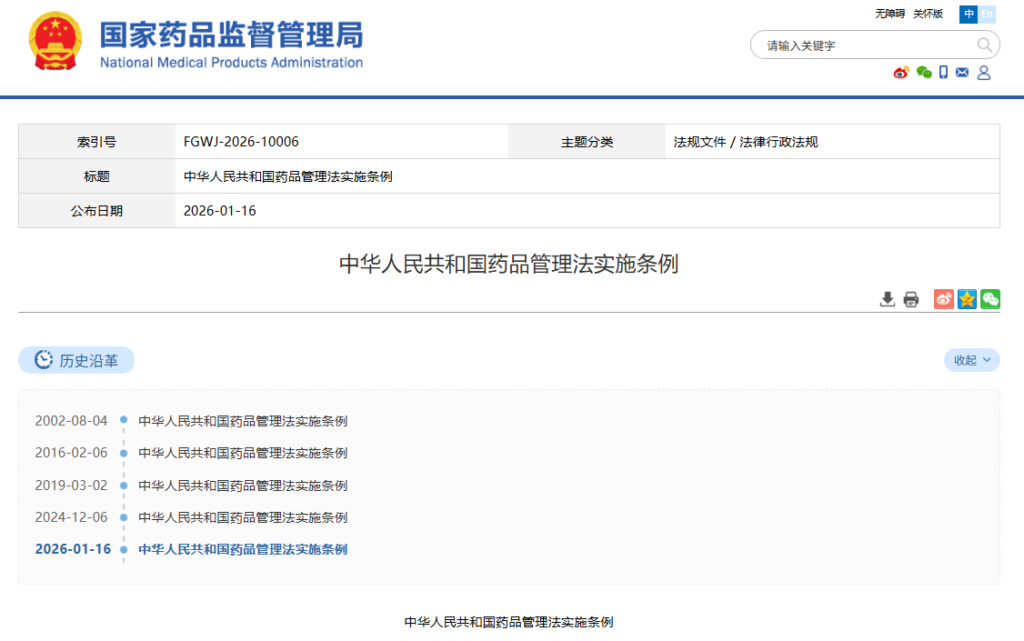
对于药企而言,这不仅意味着责任的集中,更意味着管理边界的延伸。企业必须具备对供应链各环节的实时掌控能力,尤其是在运输与仓储等外部环节中,实现对承运商资质、运输环境以及执行过程的持续监督。

在这样的背景下,“看得见的供应链”不再是管理优化的目标,而成为法律层面的基本要求。
关键能力升级:追溯与数据成为合规基础设施
新条例对药品追溯体系提出了更高标准,要求实现最小销售单元的全流程追溯,并确保数据真实、完整且可共享。这一要求,实际上将信息系统能力从“支持工具”升级为“合规基础”。
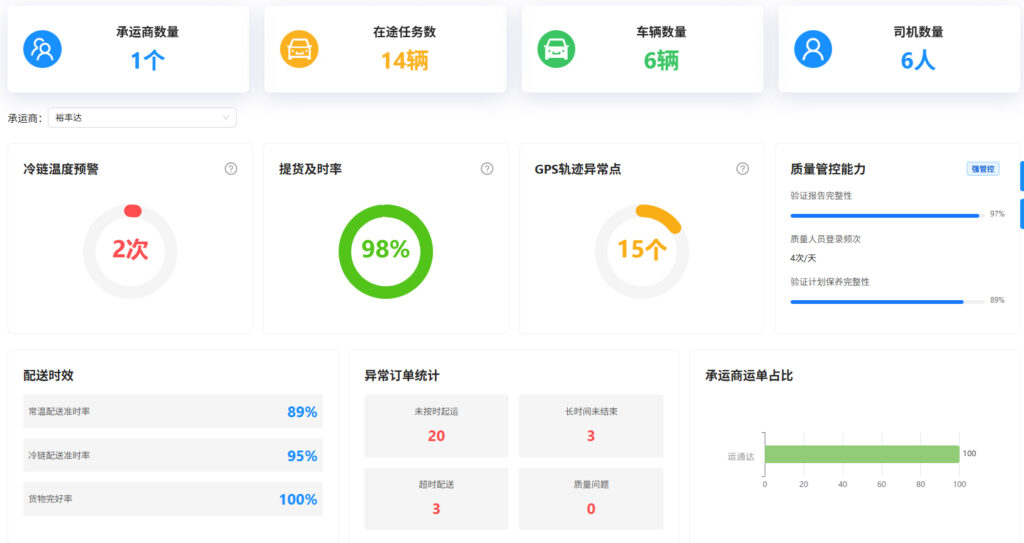
同时,法规从原则层面对药品运输过程中的温度控制、过程记录及质量可追溯性提出了要求,并强调相关数据应真实、完整、可追溯,为企业开展数字化监控与系统对接提供了监管导向。这意味着,医药物流不再只是简单的执行环节,而成为监管重点关注的高风险节点。企业如果缺乏系统化的数据采集与管理能力,将难以满足监管要求,甚至面临业务受限的风险。
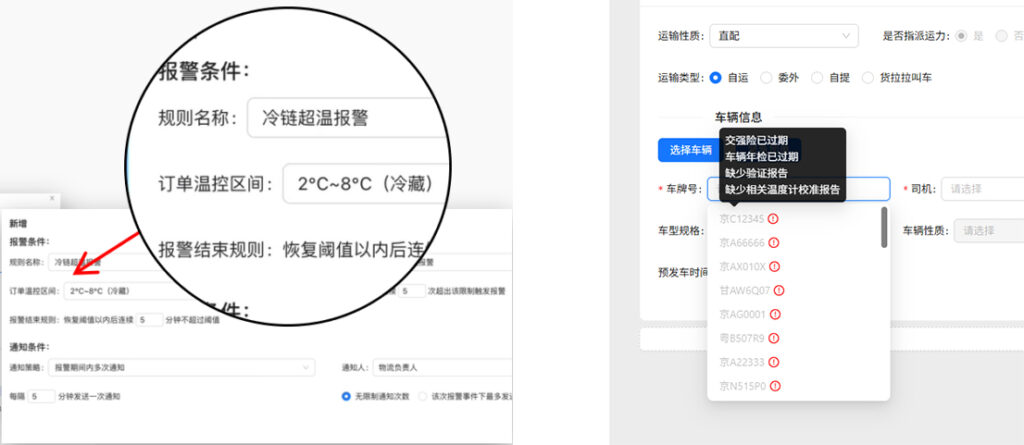
从趋势到行动:企业必须提前布局“数智化合规”
在新规正式实施之前,留给企业的准备时间正在迅速缩短。是否具备完整的追溯能力,是否能够实现数据实时对接,是否建立起对承运链条的有效管控,这些问题都将直接影响企业未来的经营资格与发展空间。
SCMsafe链四方认为,医药供应链正处于从传统管理向数智化合规转型的关键阶段。谁能率先完成这一转变,谁就能够在新一轮行业竞争中占据主动。
新规带来的不仅是压力,更是机遇。在监管与技术交汇的节点上,行业正在重新定义“合格企业”的标准。