2025年10月5日,国家标准《药品冷链物流追溯管理要求》(GB/T46204—2025)正式发布实施,这是我国医药冷链物流领域又一项重要的国家标准。该标准进一步细化了药品冷链物流追溯要求,通过建立统一的追溯体系,对温湿度监测、数据采集频率、信息保存与追溯信息等提出了明确要求,有助于快速定位问题批次、提高追溯效率、保障药品安全。
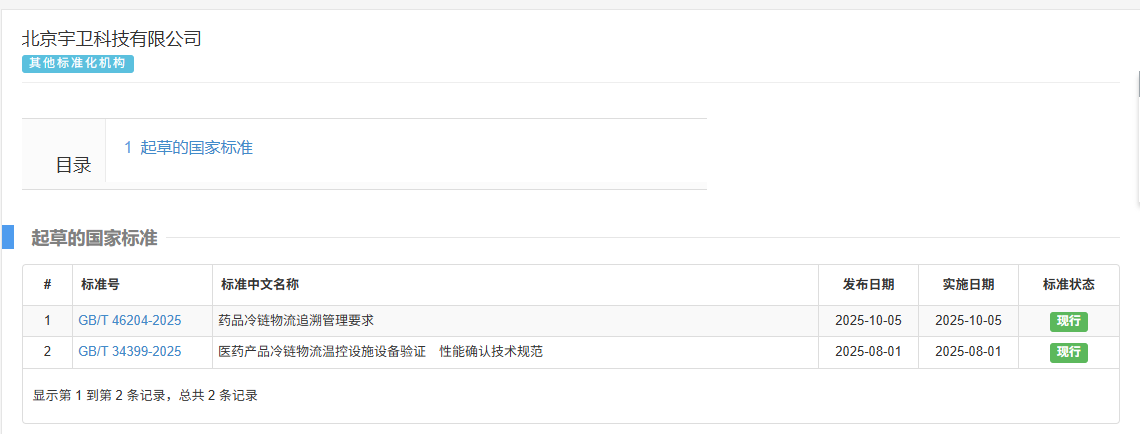
SCMsafe链四方(北京宇卫科技有限公司)作为该标准的起草单位之一,针对30多项标准内容提出了专业意见,其中被采纳的10多条。此前,SCMsafe链四方还参与起草了《医药产品冷链物流温控设施设备验证性能确认技术规范》。作为多次参与国家标准和行业标准的起草单位,SCMsafe链四方在医药物流智慧管理、医药行业数字化平台搭建、医药供应链数智化升级上体现了其专业实力和生态互联与全链路追溯技术的实施能力。
国家标准《药品冷链物流追溯管理要求》重点内容解析
1、追溯要素明确:规定必须记录的基本信息(药品/批号/生产企业/储运条件)、仓储与运输信息、委托方与收发方信息及异常处理记录;可按需扩展附加信息(设备编码、运输轨迹等)。
2、温湿度监测要求:仓储与运输均需配备合格的温湿度监测与记录设备;监测系统至少每隔1分钟更新测点数据,仓储至少每隔30分钟自动记录一次;运输至少每隔5分钟自动记录一次;超限时记录频率提高(至少每隔2分钟记录1次)。
3、设备校验与系统验证:要求定期对监测系统进行验证,对测点终端进行校准或检定,保证系统的可靠性和设备的准确性。
4、信息采集与交接流程:明确收货、入库、出库、交接时的核验与记录责任,要求在交接时确认并记录关键温度与时间节点。
5、异常记录与追溯触发:任何温湿度或药品异常必须记录并及时与委托方沟通,触发追溯的情形包括质量问题、委托方请求、药品安全事故或公共卫生事件。
6、数据保存与可检索性:追溯信息至少保存5年且不少于药品有效期满后1年;疫苗信息保存至有效期满后不少于5年;要求数据封存并能快速检索与调取。
7、追溯响应与交付:服务提供方应按协议为委托方提供追溯信息,可用任意可追溯的信息载体提交并封存相关数据。
随着国家标准《药品冷链物流追溯管理要求》的出台,与《药品经营质量管理规范》(GSP)《药品冷链物流运作规范》 等法规形成有效补充。GB/T46204-2025着重于“谁记录、如何记录、记录的内容、保存多久、如何调取”等信息链层面标准要求。把冷链安全的“温度”管理与“信息”治理并重,形成可审计、可检索、可追责的追溯体系;SCMsafe链四方作为起草单位之一,参与并推动了30多项关键条款的制定与修订,同时作为医药行业运输管理系统(TMS)软件开发的先行者,为药品冷链物流追溯管理提供了技术保障和实践路径。